Los productos Kraiburg TPE cumplen la directiva VDI 2017
Kraiburg TPE anuncia que los compuestos de su familia Thermolast M satisfacen los requisitos de la Directiva 2017 para Medical Grade Plastics (MGP), adoptada en julio de 2019 por la Asociación de Ingenieros Alemanes VDI.
03.09.2019 Como guía para los fabricantes y usuarios de plásticos destinados a productos médicos, la directiva VDI 2017 regula las exigencias que deben cumplir los grados plásticos médicos (MGP) para ser aptos: desde los requisitos básicos hasta los plazos de discontinuación, pasando por la uniformidad en la formulación y la gestión de cambios.
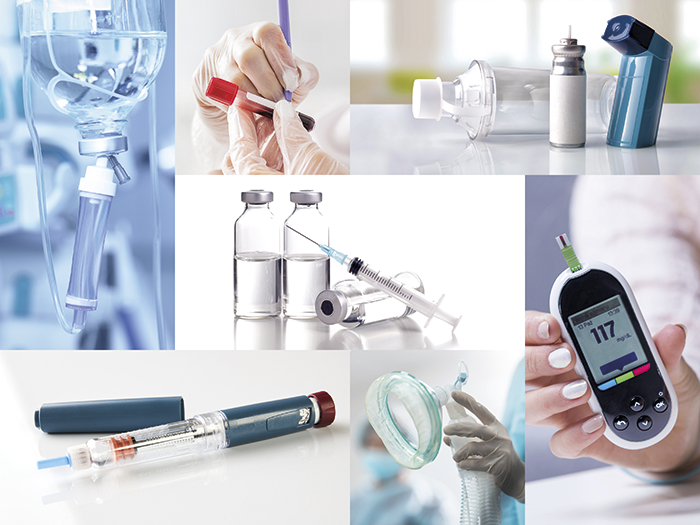
En la elaboración de la Directiva 2017 sobre Plásticos de Calidad Médica han participado 20 proveedores de materiales, usuarios y organismos notificados.
Como apuntan desde Kraiburg TPE, quitando los Drug Master Files (DMF) de la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA), la norma ISO 10993 de certificación de productos sanitarios aptos para seres humanos (incluidos implantes, sistemas de diagnóstico in vitro y envases farmacéuticos) y el Reglamento 2017/745 de la UE sobre los Productos Sanitarios, que tendrá carácter vinculante a partir de mayo de 2020, hasta hoy no existen en la UE ni en los EE.UU. directivas o normas claras para los polímeros utilizados en este campo vital de aplicaciones.
La VDI 2017 es un importante primer paso hacia la armonización del espectro de prestaciones que debe satisfacer un plástico de calidad médica, y crea orientaciones vinculantes en la comunicación entre los fabricantes de MGP y los fabricantes de productos médicos, farmacéuticos y sistemas in vitro, dice Oliver Kluge, miembro de la Comisión de la Directiva y asesor de productos sanitarios en Kraiburg TPE.
Dentro de este marco, la nueva Directiva deja espacio expresamente para la realización de acuerdos más amplios entre los proveedores de los respectivos materiales y los clientes.
Detalles de la directiva VDI 2017
Uno de los principales efectos de la VDI 2017 consiste en que limita la selección de las materias primas y auxiliares admitidas para los MGP, lo que obliga a algunos fabricantes de materiales a adaptar sus formulaciones.
Además, la nueva Directiva regula la constancia controlada de la composición de compuestos específicos sobre la base de una gestión de cambios documentada (Change Control), que garantiza su aptitud a largo plazo y hace innecesarias las costosas revisiones.
Por otra parte, la VDI 2017 prevé transiciones más largas para los materiales discontinuados y ofrece así una mayor seguridad de suministro a los usuarios.
Nuestros elastómeros termoplásticos de la familia Thermolast M para aplicaciones médicas se ajustan desde hace tiempo a las exigencias que ahora se establecen para los MGP, por lo que solo tuvimos que aumentar la precisión en unas pocas especificaciones, explica Kluge, quien asegura que seguirán colaborando activamente en las futuras revisiones de la Directiva.
De hecho, la Comisión de la Directiva 2017 sobre Plásticos de Calidad Médica prevé realizar ya en 2020 una primera revisión de la versión actual.
Compuestos Thermolast M
Todos los compuestos Thermolast M se fabrican sin metales pesados, látex, PVC ni ftalatos, con la máxima pureza y en instalaciones equipadas especialmente a tal efecto.
Los tipos de materiales seleccionados han sido probados y homologados de acuerdo con las normas USP Clase VI (Capítulo 88), ISO 10993-5 (Citotoxicidad), ISO 10993-10 (Irritación intracutánea), ISO 10993-11 (Toxicidad sistémica aguda) e ISO 10993-4 (Hemólisis).
El control de calidad de las materias primas utilizadas también incluye la completa trazabilidad de los lotes en los proveedores.
Además, los materiales de Kraiburg TPE satisfacen los requisitos fijados por el reglamento relativo al registro, la evaluación, la autorización y la restricción de las sustancias y preparados químicos (REACH) y la directiva sobre restricciones a la utilización de determinadas sustancias peligrosas (RoHS).
La gama de productos de Thermolast M aparece listada en los Drug Master Files (DMF) de la FDA, a fin de documentar las fórmulas de acuerdo con un Sistema de Control de Cambios de carácter obligatorio.
En conformidad con la nueva Directiva VDI 2017, Kraiburg TPE garantiza asimismo que los procesos de fabricación se incorporarán a la gestión de cambios y que la fórmula original de los compuestos en cuestión seguirá estando disponible al menos durante 24 meses de manera paralela al nuevo tipo después de que se notifique cualquier modificación o discontinuación.
Este mecanismo optimiza el control de calidad y asegura el suministro de los compuestos médicos de TPE a todos los clientes que se encuentran vinculados al área de la salud, al campo del diagnóstico y a la tecnología médica y farmacéutica.
*Para más información: www.kraiburg-tpe.com