Una enzima para mejorar el reciclaje de plásticos
Investigadores de la Tokyo University of Science han descubierto cómo una enzima termosensible, la cutinasa, puede mejorar el reciclaje de plásticos.
Entre los diversos métodos de reciclaje de plásticos que se están estudiando, se encuentra el reciclaje biológico de plásticos, o biorreciclaje. Este método utiliza enzimas o microorganismos para descomponer las moléculas de polímero.
Precisamente, un grupo de enzimas que está llamando la atención de la comunidad científica son las cutinasas microbianas. Estas enzimas son producidas naturalmente por bacterias y hongos para degradar la capa cerosa externa de las plantas, conocida como cutícula. Debido a que pueden actuar sobre enlaces químicos similares, se consideran prometedoras para el reciclaje de politereftalato de etileno (PET), un plástico muy utilizado en botellas y fibras sintéticas.
Sin embargo, la aplicación de estas enzimas en entornos industriales no es sencilla. El PET se degrada de forma más eficiente a temperaturas cercanas a los 70 °C, donde se vuelve más flexible y fácil de procesar. A temperaturas tan elevadas, las enzimas deben mantener una estructura general estable para evitar su desnaturalización, a la vez que conservan la flexibilidad en su sitio activo para el reconocimiento molecular y la catálisis. Esto supone un reto de diseño, ya que la rigidez estructural y la flexibilidad suelen ser propiedades opuestas.
La investigación de la Tokyo University of Science
Para comprender mejor este equilibrio, un equipo de investigadores liderado por el profesor Tatsuya Nishino del Departamento de Ciencias y Tecnología Biológicas de la Universidad de Ciencias de Tokio (TUS), junto con el profesor adjunto Sho Ito del mismo departamento y los investigadores de posgrado Ryohei Nojima (Máster en Ciencias, 2022) y Lirong Chen (Máster en Ciencias, 2024) de la TUS, examinó una enzima cutinasa termotolerante del hongo Chaetomium thermophilum.
La enzima, conocida como CtCut, se analizó en condiciones relevantes para el reciclaje de PET a altas temperaturas con el fin de comprender mejor cómo mantiene su estabilidad estructural y su potencial catalítico. El estudio se publicó en el volumen 16, número especial 4 de la revista Crystals el pasado 24 de marzo de 2026.
“Los residuos plásticos se han convertido en un grave problema en los últimos años, lo que exige tecnologías de reciclaje respetuosas con el medio ambiente. Por ello, nuestro objetivo era contribuir al desarrollo de tecnologías de reciclaje prácticas, esclareciendo la base molecular de las enzimas que funcionan incluso a altas temperaturas”, afirma el profesor Nishino.
Para el estudio, el equipo creó varias versiones de la enzima. Entre ellas, la de tipo silvestre (CtCutWT), que es la forma no modificada, y una versión mutante, CtCutS136A, en la que el aminoácido serina en la posición 136 se sustituye por alanina.
Más detalles del estudio
Posteriormente, determinaron la estructura de la enzima y evaluaron su estabilidad térmica mediante calorimetría diferencial de barrido, calentando la proteína de 30 °C a 100 °C para analizar su absorción de calor.
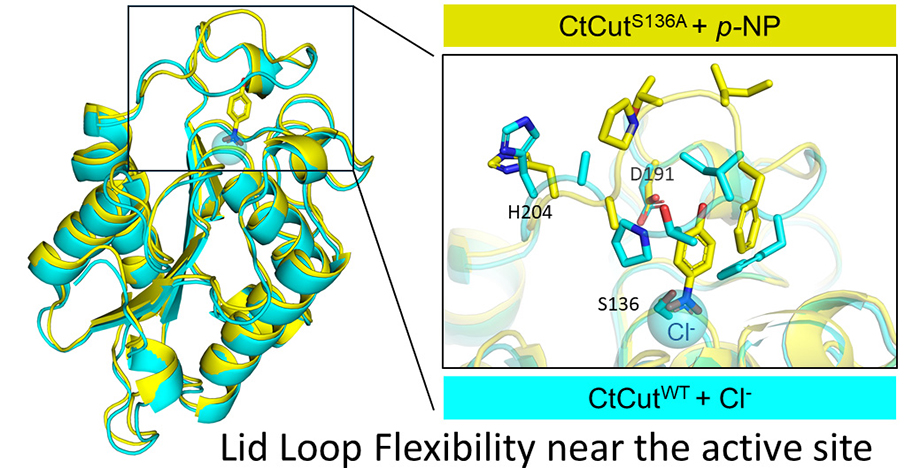
Estructuralmente, la enzima adopta un plegamiento α/β-hidrolasa altamente estable, una arquitectura común entre las cutinasas. El sitio activo está cubierto por un bucle flexible que puede abrirse y cerrarse. En su estado cerrado, el sitio activo es menos accesible, pero al unirse a una molécula, el bucle cambia de forma para permitir la unión y la catálisis.
Cabe destacar que se encontró un ion cloruro cerca del sitio activo incluso en ausencia de sustrato. Ello sugiere que el sitio activo forma un microambiente electrostático con carga positiva que podría facilitar la unión del ligando.
Al calentar la enzima, se observó un proceso de desplegamiento en dos etapas, con una transición gradual que comienza alrededor de los 60 °C. Le sigue una segunda transición cerca de los 65-70 °C. Esto indica que diferentes partes de la enzima pierden estabilidad a distintas temperaturas, lo que sugiere la presencia de regiones estructuralmente distintas dentro de la proteína.
“Nuestros hallazgos sugieren la posibilidad de una división funcional dentro de la enzima. Observamos que la región móvil cercana al sitio activo experimenta cambios estructurales en respuesta a la unión del ligando, y que la desnaturalización térmica se produce en múltiples etapas”, afirma el profesor Nishino.
Potencial del descubrimiento
Estos hallazgos respaldan la idea de que las enzimas diseñadas para la degradación de plásticos pueden requerir tanto una estructura general estable como un sitio activo flexible. El núcleo rígido proporciona la estabilidad térmica necesaria para soportar las condiciones industriales, mientras que el bucle flexible de la cubierta puede ayudar a la enzima a adaptarse a las moléculas unidas.
Al comprender mejor este equilibrio entre estabilidad y flexibilidad, el estudio aporta nuevas perspectivas sobre la función de las enzimas termotolerantes y cómo se pueden mejorar.
“Nuestro estudio podría conducir al desarrollo de tecnologías para la descomposición y el reciclaje eficientes del PET en el futuro, al proporcionar pautas de diseño para enzimas que posean tanto resistencia al calor como potencial capacidad catalítica para la degradación de polímeros. Esto podría abordar el creciente desafío de los residuos plásticos y contribuir a la consecución de una sociedad sostenible de reciclaje de recursos”, concluye el profesor Nishino.
*Para más información: Estudio publicado – https://www.tus.ac.jp/en/